
Учебник «Химия» для 10 класса, написанный Габриеляном и Остроумовым, является надежным и современным пособием, которое помогает старшеклассникам углубить свои знания в области химии. Книга отличается четкой структурой, логичным изложением материала и наглядными иллюстрациями, что способствует лучшему усвоению сложных тем. В ней рассматриваются ключевые концепции, такие как органическая и неорганическая химия, а также основы химической кинетики и термодинамики. Учебник не только помогает подготовиться к экзаменам, но и вдохновляет на дальнейшее изучение науки, делая процесс обучения увлекательным и доступным для каждого ученика.
ГДЗ по Химии 10 Класс Параграф 12 Лабораторный эксперимент 2 Габриелян, Остроумов — Подробные Ответы
Налейте в пробирку 2 мл 10%-ного раствора гидроксида натрия, добавьте несколько капель раствора сульфата меди(II). Что наблюдаете? К полученному осадку добавьте 5–6 капель глицерина и встряхните смесь. Что наблюдаете?
Этап 1: Получение реактива
Для проведения качественной реакции сначала необходимо получить свежий осадок гидроксида меди (II). Это происходит при взаимодействии соли меди со щелочью.
Уравнение реакции:
2NaOH + CuSO₄ → Na₂SO₄ + Cu(OH)₂↓
Что наблюдаем:
При смешивании бесцветного раствора щелочи (гидроксида натрия) и голубого раствора медного купороса (сульфата меди) мгновенно образуется объемный осадок ярко-синего цвета.
Этап 2: Качественная реакция на многоатомные спирты
Когда к полученному синему осадку добавляют глицерин, происходит специфическое химическое взаимодействие. Глицерин, имея три гидроксильные группы (-OH), «захватывает» ион меди, образуя устойчивое комплексное соединение.
Уравнение реакции:
Структурное описание процесса:
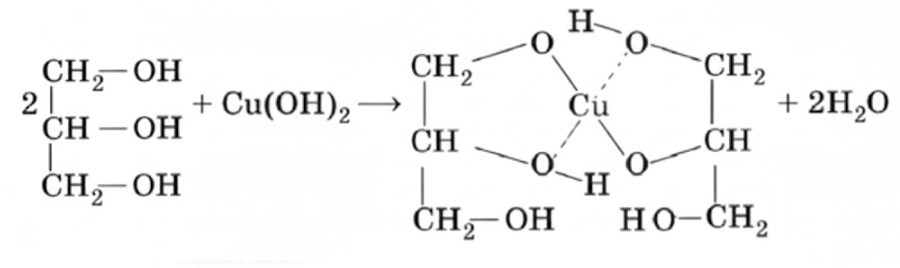
Две молекулы глицерина взаимодействуют с одной молекулой гидроксида меди (II). Атом меди замещает атомы водорода в гидроксильных группах глицерина и дополнительно связывается с соседними кислородными атомами (образуется хелатный комплекс).
Что наблюдаем:
Синий осадок полностью растворяется. Вместо него образуется прозрачный раствор темно-синего (василькового) цвета — глицерат меди (II).
Вывод: Данная реакция является качественной. Появление прозрачного ярко-синего раствора при добавлении Cu(OH)₂ однозначно доказывает, что в пробирке находится многоатомный спирт.
Этот химический опыт является классическим методом определения многоатомных спиртов. В химии его называют качественной реакцией, так как он позволяет «узнать» вещество по характерному изменению цвета и состояния раствора.
Вот подробный разбор того, что происходит на каждом этапе эксперимента.
Этап 1: Создание «реактива-индикатора»
Для обнаружения глицерина нам нужен свежеосажденный гидроксид меди (II). Его нельзя просто взять с полки в виде порошка, так как при хранении он теряет свою химическую активность. Поэтому его готовят прямо перед опытом.
Уравнение реакции:
2NaOH + CuSO₄ → Na₂SO₄ + Cu(OH)₂↓
Что происходит химически:
В этом процессе происходит реакция ионного обмена. Ионы меди (Cu²⁺) из сульфата меди встречаются с гидроксид-ионами (OH⁻) из щелочи. В результате образуется нерастворимое в воде основание — Cu(OH)₂. Мы видим это как появление ярко-синего студенистого осадка.
Этап 2: Растворение осадка глицерином
Когда мы добавляем к этому синему осадку глицерин и встряхиваем пробирку, происходит удивительное превращение: твердый осадок исчезает, а жидкость окрашивается в интенсивный темно-синий (васильковый) цвет.
Уравнение реакции:
Подробный механизм:
1. Кислотные свойства: В этой реакции глицерин проявляет очень слабые кислотные свойства. Его гидроксильные группы (-OH) взаимодействуют с гидроксидом меди.
2. Хелатирование (образование кольца): Это самая интересная часть. Молекулы глицерина как бы «обхватывают» атом меди с двух сторон, образуя устойчивую циклическую структуру (комплексное соединение). На картинке это показано пунктирными линиями — это дополнительные связи, которые удерживают медь внутри «замка» из молекул глицерина.
3. Результат: Полученное вещество — глицерат меди (II) — в отличие от исходного гидроксида, прекрасно растворяется в воде. Именно поэтому мутный осадок превращается в прозрачный ярко-синий раствор.
Почему это важно?
Эта реакция специфична. Она работает только с теми спиртами, у которых есть несколько групп -OH у соседних атомов углерода.
- Обычный спирт (этанол): Имеет только одну группу -OH. Он не сможет «растворить» синий осадок меди.
- Глицерин: Имеет три группы -OH. Он легко образует комплекс и дает синее окрашивание.
Этот опыт доказывает наличие в молекуле вещества нескольких гидроксильных групп, расположенных близко друг к другу.

Любой навык лучше отрабатывать самостоятельной практикой, и решение задач — не исключение. Прежде чем обратиться к подсказкам, стоит попробовать справиться с заданием, опираясь на свои знания. Если дойти до конца удалось — проверить ответ и в случае расхождений сверить своё решение с правильным.




Оставь свой отзыв 💬
Комментариев пока нет, будьте первым!