
Учебник «Химия» для 10 класса, написанный Габриеляном и Остроумовым, является надежным и современным пособием, которое помогает старшеклассникам углубить свои знания в области химии. Книга отличается четкой структурой, логичным изложением материала и наглядными иллюстрациями, что способствует лучшему усвоению сложных тем. В ней рассматриваются ключевые концепции, такие как органическая и неорганическая химия, а также основы химической кинетики и термодинамики. Учебник не только помогает подготовиться к экзаменам, но и вдохновляет на дальнейшее изучение науки, делая процесс обучения увлекательным и доступным для каждого ученика.
ГДЗ по Химии 10 Класс Параграф 14 Вопрос 6 Габриелян, Остроумов — Подробные Ответы
В двух пробирках без этикеток находятся растворы этиленгликоля и уксусного альдегида. Как при помощи растворов сульфата меди(II) и гидроксида натрия распознать предложенные вещества? Укажите признаки реакций.
При взаимодействии соли меди с щелочным раствором образуется синий осадок гидроксида меди (II):
2NaOH + CuSO₄ → Na₂SO₄ + Cu(OH)₂↓
Если к полученному осадку добавить уксусный альдегид и нагреть, цвет осадка изменится с синего на красный благодаря образованию оксида меди (I):
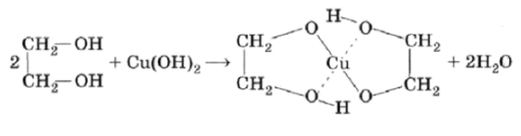
При добавлении этиленгликоля к осадку происходит растворение гидроксида меди (II), в результате чего образуется синий раствор:
Для того чтобы различить этиленгликоль и уксусный альдегид, нам понадобится свежеприготовленный гидроксид меди(II). Это универсальный реагент в органической химии, который по-разному ведет себя с многоатомными спиртами и альдегидами.
Ниже представлен подробный разбор всех этапов химического анализа с соответствующими уравнениями реакций.
Этап 1: Получение реактива
Поскольку гидроксид меди(II) неустойчив при хранении, его получают непосредственно перед опытом. Для этого к раствору щелочи (NaOH) добавляют раствор сульфата меди(II).
Уравнение реакции:
2NaOH + CuSO₄ → Na₂SO₄ + Cu(OH)₂↓
Признак: Образуется студенистый осадок ярко-синего цвета. Полученную смесь распределяют по двум пробиркам с неизвестными веществами.
Этап 2: Распознавание этиленгликоля
При добавлении этиленгликоля к осадку гидроксида меди(II) реакция происходит уже при комнатной температуре. Как многоатомный спирт, этиленгликоль образует с медью растворимое комплексное соединение.
Уравнение реакции:
Признак: Синий осадок растворяется, и получается прозрачный раствор интенсивного васильково-синего цвета. Это качественная реакция на наличие соседних гидроксильных групп (-OH).
Этап 3: Распознавание уксусного альдегида
В отличие от спирта, уксусный альдегид не реагирует с гидроксидом меди(II) на холоду. Чтобы увидеть изменения, пробирку необходимо нагреть. В ходе реакции альдегид окисляется до кислоты, а медь восстанавливается.
Уравнение реакции:
Признаки:
1. При нагревании синий цвет исчезает.
2. Образуется плотный кирпично-красный осадок оксида меди(I) — Cu₂O.
Итоговая таблица признаков
Здесь наглядно показано, как визуально отличить одно вещество от другого:
| Вещество | Реагент | Условие | Результат (признак) |
|---|---|---|---|
| Этиленгликоль | Cu(OH)₂ | Без нагревания | Растворение осадка, ярко-синий раствор |
| Уксусный альдегид | Cu(OH)₂ | Нагревание | Выпадение кирпично-красного осадка |
Этот метод позволяет безошибочно определить содержимое пробирок, используя лишь доступные неорганические соли и щелочи.

Любой навык лучше отрабатывать самостоятельной практикой, и решение задач — не исключение. Прежде чем обратиться к подсказкам, стоит попробовать справиться с заданием, опираясь на свои знания. Если дойти до конца удалось — проверить ответ и в случае расхождений сверить своё решение с правильным.


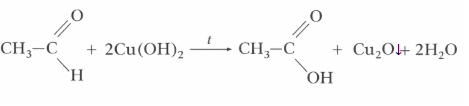


Оставь свой отзыв 💬
Комментариев пока нет, будьте первым!