
Учебник «Химия» для 10 класса, написанный Габриеляном и Остроумовым, является надежным и современным пособием, которое помогает старшеклассникам углубить свои знания в области химии. Книга отличается четкой структурой, логичным изложением материала и наглядными иллюстрациями, что способствует лучшему усвоению сложных тем. В ней рассматриваются ключевые концепции, такие как органическая и неорганическая химия, а также основы химической кинетики и термодинамики. Учебник не только помогает подготовиться к экзаменам, но и вдохновляет на дальнейшее изучение науки, делая процесс обучения увлекательным и доступным для каждого ученика.
ГДЗ по Химии 10 Класс Параграф 20 Практическая работа 1 Вариант 3 Габриелян, Остроумов — Подробные Ответы
1) Проведите реакции, характеризующие химические свойства уксусной кислоты. Опишите условия проведения и признаки реакций, составьте их уравнения. Сделайте вывод.
2) Экспериментально распознайте выданные вам в пронумерованных пробирках без этикеток вещества: растительное и машинное масла. Опишите условия проведения и признаки реакций. Сделайте вывод.
1. Химические свойства уксусной кислоты
Уксусная кислота (этановая) проявляет как общие свойства, характерные для минеральных кислот, так и специфические свойства органических карбоновых кислот.
Реакции, аналогичные неорганическим кислотам:
Для подтверждения кислотных свойств проводятся реакции с металлами, щелочами и солями.
- Взаимодействие с металлами (активнее водорода):
Zn + 2CH₃COOH → (CH₃COO)₂Zn + H₂↑
(Образуется ацетат цинка и выделяется газообразный водород) - Реакция нейтрализации (со щелочами):
NaOH + CH₃COOH → CH₃COONa + H₂O
(Взаимодействие со щелочью приводит к образованию соли — ацетата натрия и воды) - Взаимодействие с солями более слабых или летучих кислот:
- С карбонатами:
K₂CO₃ + 2CH₃COOH → 2CH₃COOK + H₂O + CO₂↑
(Наблюдается активное выделение углекислого газа) - С силикатами:
K₂SiO₃ + 2CH₃COOH → 2CH₃COOK + H₂SiO₃↓
(Выпадает характерный студенистый осадок кремниевой кислоты)
Специфические свойства органических кислот:
Уксусная кислота способна вступать в реакцию этерификации со спиртами в присутствии катализатора.
Реакция со спиртом:
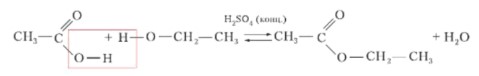
CH₃COOH + C₂H₅OH —(H₂SO₄ конц.)→ CH₃COOC₂H₅ + H₂O
(Уксусная кислота + этиловый спирт → этиловый эфир уксусной кислоты + вода)
Признак: появление приятного специфического фруктового запаха образовавшегося эфира.
Вывод: Уксусная кислота является типичной карбоновой кислотой. Она реагирует с металлами, основаниями и солями, а также образует сложные эфиры при взаимодействии со спиртами.
2. Распознавание растительного и машинного масел
Для идентификации масел в пронумерованных пробирках используется реактив на кратные (двойные) связи — бромная вода (раствор брома Br₂).
Ход определения:
- Растительное масло: В своем составе содержит остатки непредельных (ненасыщенных) жирных кислот, в молекулах которых есть двойные связи (-C=C-). При добавлении бромной воды происходит реакция присоединения.
Признак: бромная вода быстро обесцвечивается.
Схема реакции:
-CH=CH- + Br₂ → -CH(Br)-CH(Br)- - Машинное масло: Представляет собой смесь предельных углеводородов (алканов), которые не содержат двойных связей.
Признак: бромная вода сохраняет свой цвет (обесцвечивания не происходит).
Вывод: Растительное масло можно отличить от машинного по реакции с бромной водой. Обесцвечивание раствора подтверждает наличие непредельных соединений в растительном масле, в то время как машинное масло состоит из насыщенных компонентов, не вступающих в данную реакцию.
1. Исследование химических свойств уксусной кислоты
Уксусная кислота (этановая) — это «лицо» карбоновых кислот в школьном курсе. Её молекула содержит функциональную группу -COOH (карбоксильную группу), которая и определяет её поведение.
Взаимодействие с активными металлами
- Условия: Контакт кислоты с порошком или гранулами металла (например, цинка).
- Процесс: Цинк, будучи активным металлом, вытесняет водород из состава кислоты.
- Признак: Активное выделение бесцветного газа (водорода).
- Уравнение: Zn + 2CH₃COOH → (CH₃COO)₂Zn + H₂↑
- Нюанс: Образующаяся соль называется ацетатом цинка.
Реакция нейтрализации (со щелочами)
- Условия: Смешивание кислоты с раствором гидроксида натрия.
- Процесс: Ион водорода из кислоты соединяется с гидроксид-ионом щелочи, образуя воду.
- Признак: Реакция протекает с выделением теплоты. Чтобы «увидеть» её глазами, в щелочь заранее добавляют фенолфталеин (он станет малиновым), а при добавлении кислоты раствор обесцветится.
- Уравнение: NaOH + CH₃COOH → CH₃COONa + H₂O
Реакции с солями
Уксусная кислота способна вытеснять более слабые или летучие кислоты из их солей.
- С карбонатом калия:
Происходит вытеснение угольной кислоты, которая тут же распадается на воду и углекислый газ.
Признак: Бурное выделение газа («вскипание»).
Уравнение: K₂CO₃ + 2CH₃COOH → 2CH₃COOK + H₂O + CO₂↑ - С силикатом калия:
Уксусная кислота вытесняет очень слабую кремниевую кислоту.
Признак: Образование густого, бесцветного «студня» (геля).
Уравнение: K₂SiO₃ + 2CH₃COOH → 2CH₃COOK + H₂SiO₃↓
Реакция этерификации (образование эфира)
- Условия: Смешивание кислоты со спиртом (этанолом), добавление капли концентрированной серной кислоты (как водоотнимающего средства) и осторожное нагревание.
- Процесс: Молекулы кислоты и спирта «сшиваются», выделяя воду.
- Признак: Появление резкого, но приятного фруктового запаха.
- Уравнение: CH₃COOH + C₂H₅OH —(H₂SO₄, конц.)→ CH₃COOC₂H₅ + H₂O
Вывод: Уксусная кислота проявляет все свойства кислот, обусловленные подвижным атомом водорода, а также специфическую способность превращаться в сложные эфиры.
2. Экспериментальное распознавание масел
Чтобы отличить растительное масло от машинного, нужно заглянуть в их молекулярную структуру. Основное различие здесь — наличие или отсутствие «ненасыщенности» (двойных связей).
Теоретическое обоснование
- Растительное масло — это природный жир. В его составе много остатков непредельных кислот (например, олеиновой), в которых между атомами углерода есть двойные связи (-C=C-). Эти связи очень «жадные» и легко присоединяют к себе другие атомы.
- Машинное масло — это продукт переработки нефти. Оно состоит из предельных углеводородов (алканов), где все связи между углеродами одинарные (-C-C-). Они химически инертны («ленивы»).
Методика проведения опыта
В две пронумерованные пробирки добавляем бромную воду (раствор брома Br₂), которая имеет характерный желто-бурый цвет.
- В пробирке с растительным маслом:
Признак: Желтая окраска брома исчезает, раствор становится бесцветным.
Почему: Молекулы брома «разрывают» двойные связи в масле и встают на их место. Это реакция присоединения.
Схема:
-CH=CH- + Br₂ → -CH(Br)-CH(Br)- - В пробирке с машинным маслом:
Признак: Изменений нет. Бромная вода остается желтой, просто образуя слой над маслом или под ним.
Почему: В машинном масле нет двойных связей, поэтому брому просто некуда «присоединиться».
Вывод: Бромная вода является качественным реактивом на кратную связь. Её обесцвечивание в одной из пробирок однозначно указывает на растительное происхождение масла.
Сводная таблица для быстрой проверки
| Объект исследования | Реактив | Основной признак |
|---|---|---|
| Уксусная кислота | Металл (Zn) | Шипение и выделение водорода |
| Уксусная кислота | Спирт + нагрев | Запах фруктовой эссенции |
| Растительное масло | Бромная вода | Обесцвечивание (есть двойные связи) |
| Машинное масло | Бромная вода | Нет реакции (связи только одинарные) |

Любой навык лучше отрабатывать самостоятельной практикой, и решение задач — не исключение. Прежде чем обратиться к подсказкам, стоит попробовать справиться с заданием, опираясь на свои знания. Если дойти до конца удалось — проверить ответ и в случае расхождений сверить своё решение с правильным.


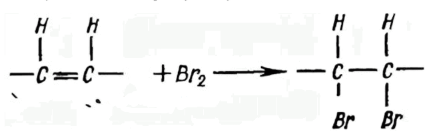


Оставь свой отзыв 💬
Комментариев пока нет, будьте первым!