
Учебник «Химия» для 10 класса, написанный Габриеляном и Остроумовым, является надежным и современным пособием, которое помогает старшеклассникам углубить свои знания в области химии. Книга отличается четкой структурой, логичным изложением материала и наглядными иллюстрациями, что способствует лучшему усвоению сложных тем. В ней рассматриваются ключевые концепции, такие как органическая и неорганическая химия, а также основы химической кинетики и термодинамики. Учебник не только помогает подготовиться к экзаменам, но и вдохновляет на дальнейшее изучение науки, делая процесс обучения увлекательным и доступным для каждого ученика.
ГДЗ по Химии 10 Класс Параграф 7 Вопрос 7 Габриелян, Остроумов — Подробные Ответы
Составьте и заполните обобщающую таблицу по теме «Углеводороды», в которой отразите следующие особенности классов этих органических соединений: состав, строение, способы получения, химические свойства, области применения.
Алканы (Предельные углеводороды)
Общие сведения
• Состав: CₙH₂ₙ₊₂
• Строение: Одинарная связь
Получение (на примере превращений бутадиена)
1. Галогенирование диенов:
CH₂=CH—CH=CH₂ + Br₂ → CH₂Br—CH=CH—CH₂Br (1,4-дибромбутен-2)
CH₂Br—CH=CH—CH₂Br + Br₂ → CH₂Br—CHBr—CHBr—CH₂Br (1,2,3,4-тетрабромбутан)
2. Гидрирование (присоединение водорода):
CH₂=CH—CH=CH₂ + H₂ (кат.) → CH₃—CH=CH—CH₃ (бутен-2)
CH₃—CH=CH—CH₃ + H₂ (кат.) → CH₃—CH₂—CH₂—CH₃ (н-бутан)
Химические свойства
• Горение: 2C₂H₆ + 7O₂ → 4CO₂↑ + 6H₂O
• Замещение (хлорирование): CH₃—CH₃ + Cl₂ → CH₃—CH₂Cl + HCl
• Дегидрирование: CH₃—CH₃ (400–600 °C, Cr₂O₃) → CH₂=CH₂ + H₂
Применение
Производство сажи и различных растворителей.
Алкены (Непредельные углеводороды)
Общие сведения
• Состав: CₙH₂ₙ
• Строение: Двойная связь (C=C)
Получение
1. Крекинг нефтепродуктов:
C₈H₁₈ (октан) → C₄H₈ (бутен) + C₄H₁₀ (бутан)
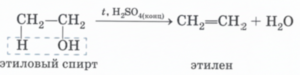
2. Дегидратация спиртов:
Химические свойства
• Горение: C₂H₄ + 3O₂ → 2CO₂↑ + 2H₂O
• Гидрогалогенирование: CH₂=CH₂ + HCl → CH₃—CH₂Cl
• Бромирование (качественная реакция):
• Гидратация: CH₂=CH₂ + H₂O (кат.) → CH₃—CH₂—OH (этиловый спирт)
• Окисление (реакция Вагнера):
(В результате образуется этиленгликоль)
Применение
Производство труб, игрушек, тары и упаковочных материалов.
Алкадиены (Углеводороды с двумя двойными связями)
Общие сведения
• Состав: CₙH₂ₙ₋₂
• Строение: C=C…C=C (две двойные связи)
Получение (на примере изопрена)
• Дегидрирование алканов:
Химические свойства (на примере бутадиена-1,3)
1. Бромирование (1,4-присоединение):
CH₂=CH—CH=CH₂ + Br₂ → CH₂Br—CH=CH—CH₂Br (1,4-дибромбутен-2)
2. Полное бромирование:
CH₂Br—CH=CH—CH₂Br + Br₂ → CH₂Br—CHBr—CHBr—CH₂Br (1,2,3,4-тетрабромбутан)
3. Гидрирование (ступенчатое):
• CH₂=CH—CH=CH₂ + H₂ (кат.) → CH₃—CH=CH—CH₃ (бутен-2)
• CH₃—CH=CH—CH₃ + H₂ (кат.) → CH₃—CH₂—CH₂—CH₃ (н-бутан)
Применение
Основная сфера — производство синтетических каучуков и последующее изготовление резины.
Алкины (Углеводороды с тройной связью)
Общие сведения
• Состав: CₙH₂ₙ₋₂
• Строение: —C≡C— (наличие тройной связи)
Получение
Основной метод получения простейшего алкина:
• Карбидный метод: CaC₂ + 2H₂O → HC≡CH↑ + Ca(OH)₂↓
Химические свойства
1. Горение: 2C₂H₂ + 5O₂ → 4CO₂↑ + 2H₂O (выделяется огромное количество тепла)
2. Присоединение хлороводорода: C₂H₂ + HCl → CH₂=CHCl (винилхлорид)
3. Бромирование (ступенчатое):
• CH≡CH + Br₂ → CHBr=CHBr (1,2-дибромэтен)
• CHBr=CHBr + Br₂ → CHBr₂—CHBr₂ (1,1,2,2-тетрабромэтан)
4. Гидратация (реакция Кучерова):
5. Окисление перманганатом калия:
Применение
Используются для автогенной сварки и резки металлов, а также как сырье для производства полимеров (например, ПВХ).
Арены
• Состав: CₙH₂ₙ₋₆.
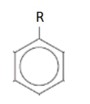
• Строение:
Получение (Реакция тримеризации)
3C₂H₂ —(уголь активиров., t)—> C₆H₆
Химические свойства
- Горение (окисление): Полное окисление бензола до углекислого газа и воды.
2C₆H₆ + 15O₂ —> 12CO₂ + 6H₂O - Хлорирование (замещение): Взаимодействие с хлором (обычно в присутствии катализатора).
C₆H₆ + Cl₂ = C₆H₅Cl + HCl (получается хлорбензол) - Нитрование: Реакция с азотной кислотой.
C₆H₆ + HNO₃ = C₆H₅NO₂ + H₂O (получается нитробензол)
Применение в промышленности
| Сфера | Что производят |
|---|---|
| Химия | Растворители, ацетон, анилин |
| Сельское хозяйство | Пестициды |
| Медицина | Лекарственные препараты |
| Быт и техника | Пластмассы |
Алканы
Состав и строение
Алканы — это предельные (насыщенные) углеводороды. Все валентности атомов углерода заняты атомами водорода.
- Состав: Общая формула CnH2n+2. Например, при C=2, H=2*2+2=6, этан C2H6.
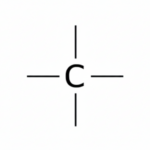
- Строение: Все связи одинарные. Углерод в sp3-гибридизации, тетраэдрическая структура с углами около 109,5°. Центральный атом C с четырьмя одинарными связями в разные стороны.
Способы получения
Получение алканов из непредельных соединений (алкадиенов и алкенов) путем насыщения.
1. Реакции с бромом (промежуточные стадии)
- CH2=CH-CH=CH2 + Br2 → CH2Br-CH=CH-CH2Br
1,4-присоединение к бутадиену-1,3. Бром атакует края цепи, двойная связь перемещается в центр, образуется 1,4-дибромбутен-2. - CH2Br-CH=CH-CH2Br + Br2 → CH2Br-CHBr-CHBr-CH2Br
Дальнейшее бромирование: двойная связь разрывается, присоединяются еще два атома брома, получается 1,2,3,4-тетрабромбутан.
2. Гидрирование (прямое получение алканов)
- CH2=CH-CH=CH2 + H2 (кат.) → CH3-CH=CH-CH3
Частичное гидрирование бутадиена-1,3. Добавляется одна молекула водорода, диен превращается в алкен (бутен-2). - CH3-CH=CH-CH3 + H2 (кат.) → CH3-CH2-CH2-CH3
Полное гидрирование. Бутен-2 поглощает еще одну молекулу водорода, двойная связь исчезает, образуется н-бутан.
Химические свойства
Алканы химически пассивны, но участвуют в важных реакциях при определенных условиях.
1. Горение (Окисление)
- 2C2H6 + 7O2 → 4CO2↑ + 6H2O
Полное окисление этана с выделением большого количества тепла. Основа мирового топлива.
2. Галогенирование (Замещение)
- CH3-CH3 + Cl2 → CH3-CH2Cl + HCl
Радикальное замещение под действием света: один атом водорода заменяется на хлор, образуются хлорэтан и хлороводород.
3. Дегидрирование
- CH3-CH3 (400-600 °C, Cr2O3) → CH2=CH2 + H2
При нагревании с катализатором этан теряет водород, образуется этилен — сырьё для пластмасс.
Применение
- Производство сажи — при неполном сгорании или термическом разложении метана, используется для шин и красок.
- Растворители — жидкие алканы (гексан) растворяют жиры и масла, применяются в химчистке и лакокрасочной промышленности.
- Топливо — природный газ, бензин и керосин состоят преимущественно из алканов.
Алкены
Состав и строение
Алкены — непредельные (ненасыщенные) углеводороды с одной двойной связью между атомами углерода.
- Состав: Общая формула CnH2n. Например, при C=2, H=4 — этилен C2H4.
- Строение: Двойная связь C=C состоит из прочной σ-связи и менее прочной π-связи, которая легко разрывается, обеспечивая высокую реакционную способность.
Способы получения
Два основных метода получения алкенов:
- Крекинг алканов:
C8H18 (октан) —(t)→ C4H8 (бутен) + C4H10 (бутан)
Под действием высокой температуры длинная молекула алкана разламывается на алкен и алкан. Это основной промышленный способ получения. - Дегидратация спиртов:
При нагревании спирта с концентрированной серной кислотой отщепляется вода, образуется двойная связь между углеродами.
Химические свойства
Алкены активно вступают в реакции присоединения благодаря двойной связи.
- Горение:
C2H4 + 3O2 → 2CO2↑ + 2H2O
Полное окисление этилена с образованием углекислого газа и воды. - Гидрогалогенирование:
CH2=CH2 + HCl → CH3-CH2Cl
Присоединение хлороводорода с разрывом двойной связи, образуется хлорэтан. - Галогенирование (бромирование):
Качественная реакция: бромная вода обесцвечивается, бром присоединяется по месту двойной связи. - Гидратация:
CH2=CH2 + H2O —(кат.)→ CH3-CH2-OH
Присоединение воды с образованием этилового спирта. - Мягкое окисление (Реакция Вагнера):
Двойная связь разрывается, к каждому атому углерода присоединяется OH-группа. Образуется этиленгликоль, марганцовка обесцвечивается, выпадает бурый осадок MnO2.
Применение
- Производство полимеров (полиэтилен, полипропилен).
- Изготовление бытовых товаров: трубы, детские игрушки, пищевая тара, упаковочная пленка.
Алкадиены
Состав и строение
Алкадиены — непредельные углеводороды с двумя двойными связями.
- Состав: Общая формула CnH2n−2. Совпадает с алкинами, но строение отличается.
- Строение: Наличие двух двойных связей C=C…C=C. Важны сопряжённые диены, где двойные связи разделены одной одинарной связью, что придаёт особые свойства.
Способы получения
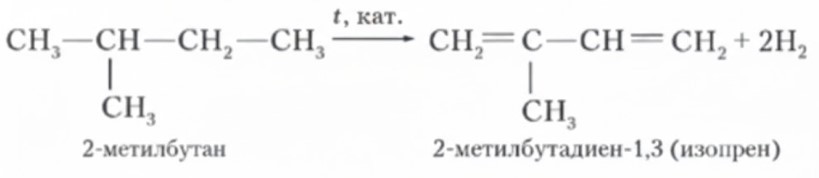
Основной метод — дегидрирование разветвленных алканов.
Реагент: 2-метилбутан (изопентан).
Продукт: 2-метилбутадиен-1,3 (изопрен) и водород.
Высокая температура и катализатор отрывают 4 атома водорода, образуются две двойные связи.
Изопрен — важное сырьё для каучука.
Химические свойства
Характерны реакции присоединения, зависящие от условий.
- Галогенирование (присоединение брома):
CH2=CH-CH=CH2 + Br2 → CH2Br-CH=CH-CH2Br
1,4-присоединение: бромы присоединяются к 1 и 4 атомам углерода, двойная связь сдвигается в центр, образуется 1,4-дибромбутен-2.
CH2Br-CH=CH-CH2Br + Br2 → CH2Br-CHBr-CHBr-CH2Br
При избытке брома двойная связь разрывается полностью, образуется 1,2,3,4-тетрабромбутан. - Гидрирование (присоединение водорода):
CH2=CH-CH=CH2 + H2 —(кат.)—> CH3-CH=CH-CH3
Частичное гидрирование: диен превращается в алкен (бутен-2).
CH3-CH=CH-CH3 + H2 —(кат.)—> CH3-CH2-CH2-CH3
Полное гидрирование: бутен-2 превращается в алкан — н-бутан.
Применение
- Основное применение — производство резины.
- Алкадиены (бутадиен, изопрен) полимеризуют, получая синтетический каучук.
- Вулканизация превращает каучук в прочную эластичную резину для шин, обуви и бытовых изделий.
Алкины
Состав и строение
Алкины — непредельные углеводороды с одной тройной связью между атомами углерода.
- Состав: Общая формула CnH2n−2. На 4 атома водорода меньше, чем в соответствующих алканах (например, этан C2H6, этин C2H2).
- Строение: Группа -C≡C-. Углероды в sp-гибридизации, молекула линейная, тройная связь состоит из одной σ- и двух π-связей.
Получение
Классический метод получения ацетилена:
- CaC2 + 2H2O → HC≡CH↑ + Ca(OH)2↓
Карбид кальция реагирует с водой, выделяя ацетилен и образуя осадок гидроксида кальция.
Химические свойства
Алкины активны в реакциях присоединения и окисления.
- Горение (Окисление):
2C2H2 + 5O2 → 4CO2↑ + 2H2O
Ацетилен горит с высокой температурой пламени, используется для сварки металлов. - Гидрохлорирование:
C2H2 + HCl → CH2=CHCl
Присоединение хлороводорода с разрывом одной π-связи, образуется винилхлорид — сырьё для ПВХ. - Галогенирование (Присоединение брома):
CH≡CH + Br2 → CHBr=CHBr (1,2-дибромэтен)
CHBr=CHBr + Br2 → CHBr2-CHBr2 (1,1,2,2-тетрабромэтан)
Бромная вода обесцвечивается — качественная реакция. - Гидратация (Реакция Кучерова):
Присоединение воды с образованием уксусного альдегида (этаналя). - Жесткое окисление марганцовкой:
Тройная связь полностью разрывается, образуется щавелевая кислота, выпадает бурый осадок MnO2, образуется щелочь.
Применение
- Сварка металлов благодаря высокой температуре горения ацетилена.
- Производство полимеров: винилхлорид для ПВХ, искусственные волокна, каучуки.
- Органический синтез: уксусная кислота, растворители, лекарственные средства.
Арены
Состав и строение
Арены — циклические углеводороды с устойчивой системой — бензольным кольцом.
- Состав: Общая формула CnH2n−6, что отражает дефицит водорода из-за циклической структуры и сопряжённых связей.
- Строение: Шестиугольник с кругом внутри и радикалом R — символ бензольного кольца. Все шесть атомов углерода в sp2-гибридизации, образуют плоский шестиугольник. Шесть π-электронов создают ароматическую систему, придающую молекуле высокую устойчивость.
Получение
Классический метод синтеза бензола из ацетилена:
- 3C2H2 —(уголь активиров., t)—> C6H6
Тримеризация ацетилена (реакция Зелинского). При пропускании ацетилена над активированным углем при ~600 °C три молекулы объединяются в бензол.
Химические свойства
Арены неохотно вступают в реакции присоединения, характерны реакции замещения, сохраняющие бензольное кольцо.
- Горение (Окисление):
2C6H6 + 15O2 → 12CO2↑ + 6H2O
Полное окисление бензола. При недостатке кислорода горит коптящим пламенем с образованием сажи. - Хлорирование (Замещение):
C6H6 + Cl2 = C6H5Cl + HCl
Электрофильное замещение одного атома водорода на хлор с катализатором (например, FeCl3), образуется хлорбензол и хлороводород. - Нитрование (Замещение):
C6H6 + HNO3 = C6H5NO2 + H2O
Взаимодействие с азотной кислотой (часто с концентрированной серной кислотой). Водород замещается нитрогруппой (-NO2), получается нитробензол с характерным запахом.
Применение
- Растворители: бензол, толуол, ксилолы для лаков, красок и смол.
- Синтез органических веществ: ацетон, анилин (для красителей), фенол.
- Сельское хозяйство: производство пестицидов и гербицидов.
- Медицина: синтез лекарств, например аспирина.
- Материалы: пластмассы, синтетические волокна, взрывчатые вещества.

Любой навык лучше отрабатывать самостоятельной практикой, и решение задач — не исключение. Прежде чем обратиться к подсказкам, стоит попробовать справиться с заданием, опираясь на свои знания. Если дойти до конца удалось — проверить ответ и в случае расхождений сверить своё решение с правильным.


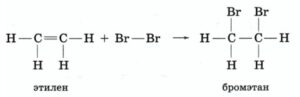





Оставь свой отзыв 💬
Комментариев пока нет, будьте первым!