
Учебник «Химия» для 8-го класса, написанный Габриеляном и Остроумовым, представляет собой качественное учебное пособие, которое помогает школьникам погрузиться в мир химии и освоить ее основные понятия. Книга отличается доступным языком изложения, продуманной структурой и ярким оформлением, что делает процесс изучения увлекательным и понятным.
ГДЗ по Химии 8 Класс Параграф 20 Вопрос 7 Габриелян, Остроумов — Подробные Ответы
Придумайте и решите задачу на нахождение объёма кислорода (н. у.), выделившегося при каталитическом разложении пероксида водорода \( \text{H}_2\text{O}_2 \).
Дано:
n(H₂O₂) = 5 моль
Vₘ = 22,4 л/моль
V(O₂) = ?
Реакция:
\(2H_2O_2 \rightarrow 2H_2O + O_2 \uparrow\)
По уравнению реакции:
| H₂O₂ | O₂ |
|---|---|
| 5 моль | x моль |
| 2 молекулы | 1 молекула |
\( x = n(O_2) = \frac{5}{2} = 2,5 \text{ моль} \)
\( V(O_2) = n \cdot V_m = 2,5 \cdot 22,4 = 56 \text{ л} \)
Ответ: 56 л.
1. Запишем уравнение химической реакции:
Каталитическое разложение пероксида водорода (\(\text{H}_2\text{O}_2\)) — это процесс, при котором он распадается на воду и газообразный кислород. Уравнение этой реакции выглядит следующим образом:
Стрелка вверх (\(\uparrow\)) указывает на выделение газа.
2. Определим известные и искомые величины:
- Нам дано количество вещества пероксида водорода, которое вступило в реакцию: \(n(\text{H}_2\text{O}_2) = 5 \text{ моль}\).
- Нам нужно найти объем кислорода (\(V(\text{O}_2)\)), который выделился в результате реакции. Указано, что объем нужно найти при нормальных условиях (н.у.).
- При нормальных условиях (температура 0°C и давление 1 атмосфера) один моль любого газа занимает объем, равный 22,4 литра. Это так называемый молярный объем газа (\(V_m\)). То есть, \(V_m = 22,4 \text{ л/моль}\).
3. Используем стехиометрические соотношения по уравнению реакции:
Из сбалансированного уравнения реакции \(2\text{H}_2\text{O}_2 \rightarrow 2\text{H}_2\text{O} + \text{O}_2\) видно, что 2 моль пероксида водорода разлагаются с образованием 1 моль кислорода.
Это означает, что количество вещества образовавшегося кислорода будет в два раза меньше, чем количество вещества разложившегося пероксида водорода.
Мы можем найти количество моль кислорода (\(n(\text{O}_2)\)) с помощью пропорции:
Если \(2 \text{ моль } \text{H}_2\text{O}_2\) дают \(1 \text{ моль } \text{O}_2\),
то \(5 \text{ моль } \text{H}_2\text{O}_2\) дадут \(x \text{ моль } \text{O}_2\).
\(x = n(\text{O}_2) = \frac{5 \text{ моль } \text{H}_2\text{O}_2 \cdot 1 \text{ моль } \text{O}_2}{2 \text{ моль } \text{H}_2\text{O}_2}\)
\(n(\text{O}_2) = 2,5 \text{ моль}\).
Таким образом, при разложении 5 моль пероксида водорода образуется 2,5 моль кислорода.
4. Рассчитаем объем кислорода:
Для расчета объема газа при нормальных условиях используется формула:
\(V = n \cdot V_m\)
Где:
- \(V\) — объем газа (в литрах)
- \(n\) — количество вещества газа (в молях)
- \(V_m\) — молярный объем газа при нормальных условиях (в л/моль)
Подставим значения, которые мы определили:
\(V(\text{O}_2) = 2,5 \text{ моль} \cdot 22,4 \text{ л/моль}\)
\(V(\text{O}_2) = 56 \text{ л}\).
Ответ:
Объем выделившегося кислорода составляет 56 л.

Любой навык лучше отрабатывать самостоятельной практикой, и решение задач — не исключение. Прежде чем обратиться к подсказкам, стоит попробовать справиться с заданием, опираясь на свои знания. Если дойти до конца удалось — проверить ответ и в случае расхождений сверить своё решение с правильным.


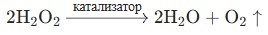



Оставь свой отзыв 💬
Комментариев пока нет, будьте первым!