
Учебник «Химия. 9 класс» О. С. Габриеляна — популярное пособие для изучения основ химии. Он выделяется доступным языком, логичной структурой и ярким иллюстративным материалом, что делает обучение понятным и интересным.
ГДЗ по Химии 9 Класс Параграф 1 Вопрос 7 Габриелян, Остроумов — Подробные Ответы
Распределите перечисленные ниже формулы веществ на четыре группы: Na2SO4, Hl, V205, KMn04, Co(OH)2, H2CrO4, NiO, CsOH, (NH4)2Cr2O7, Ca(OH)2, Cl20, HCN. Дайте названия всем веществам.
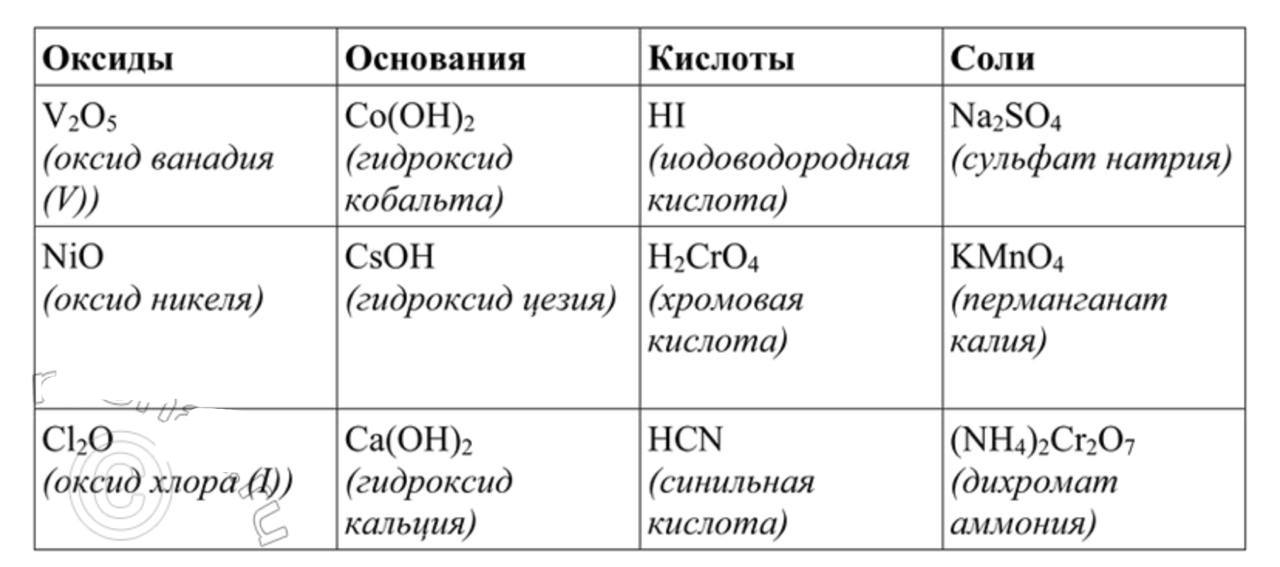
Соли:
Na₂SO₄ (натрий сульфат)
KMnO₄ (калий перманганат)
(NH₄)₂Cr₂O₇ (аммоний хромат)
Кислоты:
HCl (соляная кислота)
H₂CrO₄ (хромовая кислота)
HCN (цианистая кислота)
Основания:
CsOH (цезий гидроксид)
Ca(OH)₂ (кальций гидроксид)
Co(OH)₂ (кобальт(II) гидроксид)
Оксиды:
V₂O₅ (ванадий(V) оксид)
NiO (никель(II) оксид)
Cl₂O (оксид хлора)
1. Соли
Соли — это соединения, образующиеся в результате реакции кислоты с основанием. Они обычно имеют нейтральный pH и могут быть растворимыми или нерастворимыми в воде.
Na₂SO₄ (натрий сульфат): Это соль, образующаяся из серной кислоты (H₂SO₄) и натрий гидроксида (NaOH). Она широко используется в химической промышленности и как удобрение.
KMnO₄ (калий перманганат): Это соль, состоящая из калия и перманганат-ионов. Применяется как окислитель в химических реакциях и в медицине для дезинфекции.
(NH₄)₂Cr₂O₇ (аммоний хромат): Это соль, образующаяся из аммиака (NH₃) и хромовой кислоты (H₂CrO₄). Используется в аналитической химии и для получения хрома.
2. Кислоты
Кислоты — это вещества, которые могут отдавать протоны (H⁺) в растворе. Они имеют кислый вкус и могут реагировать с основаниями, образуя соли.
HCl (соляная кислота): Это сильная кислота, широко используемая в лабораториях и промышленности. Образуется при растворении водорода в хлоре.
H₂CrO₄ (хромовая кислота): Это сильная кислота, содержащая хром. Используется в аналитической химии и для получения различных хромовых соединений.
HCN (цианистая кислота): Это слабая кислота, содержащая цианид-ион. Является токсичным веществом и используется в производстве пластмасс и красителей.
3. Основания
Основания — это вещества, которые могут принимать протоны или отдавать гидроксид-ион (OH⁻) в растворе. Они обычно имеют щелочной вкус и могут нейтрализовать кислоты.
CsOH (цезий гидроксид): Это сильное основание, которое используется в аналитической химии и для получения цезиевых соединений.
Ca(OH)₂ (кальций гидроксид): Также известен как известковая вода. Используется в строительстве, для нейтрализации кислот и в пищевой промышленности.
Co(OH)₂ (кобальт(II) гидроксид): Это основание, которое используется в производстве кобальтовых соединений и в электронике.
4. Оксиды
Оксиды — это соединения, содержащие кислород и другой элемент. Они могут быть как кислотными, так и основными.
V₂O₅ (ванадий(V) оксид): Это оксид ванадия, который используется как катализатор в химических реакциях и в производстве стекла.
NiO (никель(II) оксид): Это основный оксид никеля, который используется в производстве никелевых батарей и как пигмент.
Cl₂O (оксид хлора): Это оксид хлора, который используется как дезинфицирующее средство и для получения других хлорсодержащих соединений.





Оставь свой отзыв 💬
Комментариев пока нет, будьте первым!